In arrivo il sì dell’Ema al vaccino Astrazeneca: dai tagli delle forniture all’efficacia sugli anziani, ecco i problemi per il piano italiano
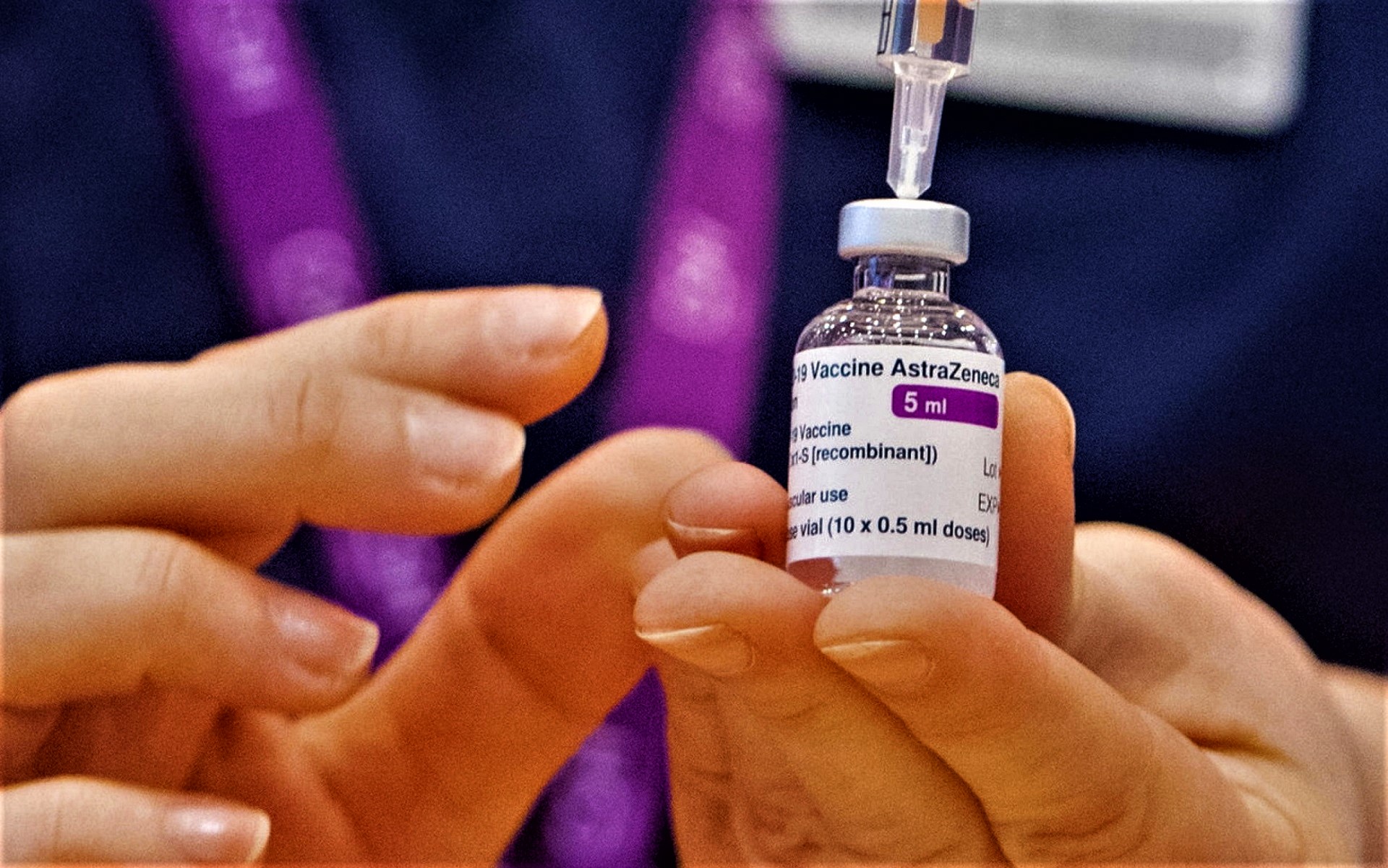

La permanenza nel limbo del vaccino Astrazeneca potrebbe avere le ore contate. Nella giornata di domani 29 gennaio finalmente l’Ema si pronuncerà sulla validità del siero anti Covid di Oxford. Se sarà ritenuto sicuro ed efficace smetterà di essere un vaccino candidato ed entrerà nella rosa delle formule finora ufficialmente autorizzate, insieme a Pfizer e Moderna. Per l’Italia sarà poi la volta, di lì a pochi giorni, del via libera di Aifa, l’Agenzia italiana del farmaco, chiamata ad autorizzare la diffusione del vaccino su territorio nazionale. Ma se nel nostro Paese l’arrivo di Astrazeneca ha da sempre fatto annunciare scenari di svolta per il piano vaccinale, le condizioni in cui ci si avvicina all’approvazione si rivelano tutt’altro che rincuoranti.
Il piano italiano rischia lo stesso di non rispettare i tempi
È bene ricordare che l’Italia su Astrazeneca ha puntato molto fin dall’inizio. Meno costoso, più facile da conservarsi, quella di Oxford era sembrata la sperimentazione più convincente su cui investire. Da qui l’accordo per 40,38 milioni di dosi in tutto, con circa 16 milioni previste per il primo trimestre. Dopo quello con Johnson & Johnson (53,84 milioni totali), il contratto più impegnativo di tutti. Ma da quel 13 giugno, giorno in cui l’Italia firmò per la prima volta insieme a Germania, Francia e Olanda, di cose ne sono cambiate. Tra problemi di sperimentazione e richieste continue di nuovi dati da parte di Ema, i 16 milioni entro il primo trimestre sono diventati 8, fino poi al taglio definitivo di tre giorni fa: – 60% di dosi in meno con solo 3,4 milioni previste entro marzo. E al piano già in crisi che succede?
Riguardo a uno dei due grandi problemi più volte evidenziati da Open, e cioè la mancanza di forniture per garantire i numeri promessi dal governo, i 3,4 milioni di dosi promesse da Astrozeneca entro marzo potrebbero arrivare a coprire, nelle stesse condizioni riconosciute anche a Pfizer e Moderna, precisamente il buco di 3.3 milioni di dosi attualmente mancanti. Un “precisamente” che non rincuora, visto la necessità sempre dichiarata dai governi di dover arrivare a una quantità di dosi disponibili in più rispetto a quelle strettamente necessarie, al fine di riuscire ad affrontare gli eventuali disguidi (e finora ce ne sono stati molti). Lo dimostra anche il progetto iniziale pensato per il primo trimestre: 28 milioni di dosi per 6.5 milioni di persone da vaccinare. Più del doppio di quelle necessarie alle due somministrazioni, e cioè 13 milioni. Ora da 28 siamo passati a solo 15 milioni di fornitura disponibile in totale, appena 2 milioni sopra lo stretto necessario.
Ma anche le condizioni di approvazione che l’Ema potrebbe imporre al vaccino di Oxford preoccupano: infatti potrebbe essere dichiarato non sicuro ed efficace per gli over 65, con un via libera che escluderebbe la categoria che più di tutte è in attesa di iniziare la prime somministrazioni. Sarebbero ancora una volta gli over 80 a rimanere fuori, così come annunciato dal governo in conseguenza dei ritardi Pfizer, e come ancora prima evidenziato da Open a prescindere dai rallentamenti. La speranza starebbe in qualche altra autorizzazione o in un accordo dell’ultima ora. Opzione quest’ultima piuttosto improbabile al momento, visti i rapporti sempre più tesi tra le aziende produttrici e la Commissione europea.
La questione degli over 65
«Non voglio pregiudicare il risultato della valutazione, perché l’analisi scientifica a livello di esperti è ancora in corso, ma sul parere per il vaccino di AstraZeneca, è possibile che venga emessa un’autorizzazione rivolta ad un gruppo di età». Lo ha detto la direttrice dell’Ema Emer Cooke, poche ore fa, proprio in riferimento all’atteso verdetto di domani sul vaccino di Oxford. Il problema starebbe nella povertà di dati che in merito alla categoria over 65 la casa farmaceutica avrebbe fornito all’ente regolatore e che Astrazeneca attraverso Pascal Soriot ha spiegato così:
La sperimentazione è stata gestita da Oxford che è un gruppo accademico molto etico, quindi non conducono test sugli anziani fino a quando non ci sono dati certi sulla sperimentazione sui giovani.
Ma secondo i responsabili della ricerca questo non costituirebbe un problema: «Sebbene i dati sugli anziani non siano abbastanza, si ritiene che comunque anche per loro ci sia un buon rapporto rischi-benefici. La cosa più importante adesso per loro è evitare innanzitutto morti, ricoveri e degenerazioni gravi del Covid, e in questo senso il nostro vaccino protegge gli over 50 e 60». Nei giorni scorsi le notizie sulla questione si sono rincorse.
Il quotidiano tedesco Handelsblatt aveva ritenuto di essere in possesso di informazioni confermate da fonti governative: «La Germania non si aspetta un’efficacia oltre l’8% tra gli over 65». In risposta era subito intervenuto a rassicurare su Astrazeneca il capo del consiglio scientifico del governo britannico, Patrick Vallance, parlando di un vaccino «sicuro ed efficace» al pari di quello Pfizer/BioNTech e assicurando una «risposta immunitaria analoga su giovani e anziani». Quello che si capirà nelle prossime ore è se le testimonianze degli altri Paesi e le rassicurazioni da parte della stessa azienda, saranno sufficienti anche per l’ente regolatore europeo, alle prese con una decisione senza dubbio complessa.
L’efficacia al 60%/70% sarà sufficiente per gli ultra ottantenni?
Un’altra questione importante è quella dell’efficacia. A differenza di Pfizer e Moderna, rispettivamente con il 95% e il 94,1% di capacità di difesa, Astrazeneca si presenta al vaglio dell’Ema con un 70,4%. La cifra è stata ottenuta dalla media di due dosaggi differenti seguiti durante la sperimentazione: quando il vaccino è stato somministrato con due dosi intere ad almeno un mese di distanza ha mostrato un’efficacia del 62%; quando invece è stato somministrato con mezza dose, seguita da una dose piena ad almeno un mese di distanza, ha mostrato un’efficacia pari al 90%. L’analisi combinata dei due regimi di dosaggio ha prodotto l’efficacia media del 70%.
Va da sé che se l’autorizzazione di Ema sarà data sulla base di una doppia somministrazione a dose completa la percentuale di efficacia a cui far riferimento è quella del 60%. Un numero sopra il 50% minimo permesso dall’Oms per i vaccini, ma non di molto come nel caso di Pfizer e Moderna. Il tema a questo punto è anche quello di scegliere quale siero utilizzare per per una delle popolazioni in assoluto più sensibili all’infezione e se garantire agli over 80 l’iniezione con la formula più sicura tra quelle attualmente approvate.
Le dosi in più di Astrazeneca non serviranno se si continua ad andare a rilento con quelle che già ci sono
«Solo fra due settimane, quando verosimilmente ci sarà stata l’approvazione del vaccino di AstraZeneca, e Pfizer tornerà a fornire a pieno regime le dosi previste, avremo a disposizione tre vaccini, insieme anche a Moderna, che ci consentiranno di completare la vaccinazione per medici e infermieri e cominciare con gli over 80». Il vice ministro alla Salute Sileri, lo stesso che nel giro di 24 ore aveva annunciato lo slittamento del piano di 4 settimane per gli over 80, di 6-8 per tutte le altre categorie, e che poi aveva invitato nuovamente a fidarsi di Pfizer, sembra ottimista sul recupero imminente della campagna. Ma anche in caso di un’autorizzazione da parte di Ema, Astrazeneca non potrà certo aiutare sull’altro grande problema del piano vaccinale, e cioè quello dei tempi. Ci saranno dosi in più (poche) ma un ritmo di somministrazione ancora insufficiente.
I 15 milioni totali di dosi (forse) disponibili entro marzo, ritardi e rallentamenti permettendo, dovranno essere distribuite al ritmo di almeno 155 mila iniezioni al giorno: solo in questo modo i 6.5 milioni di soggetti a rischio potranno avere la doppia somministrazione e quindi la completa immunità dal virus. Ad oggi viaggiamo con la media giornaliera di circa 56 mila dosi iniettate.
Una cifra, come ha fatto notare Open, non certo lontana dalla velocità tenuta anche prima dei ritardi Pfizer: 60 mila dosi giornaliere. Nel frattempo il bando indetto dal governo per la realizzazione delle “primule“, i padiglioni di vaccinazione progettati da Boeri, fa sperare in nuovi hub di somministrazione (fino a 1.200) che potrebbero aiutare ad incrementare il ritmo. La chiusura della gara ha subìto però già i primi ritardi slittando al 3 febbraio. La proroga di una settimana è stata motivata da Arcuri con i ritardi del piano vaccinale causati da Pfizer negli ultimi giorni.
Leggi anche:
- Vaccini, Astrazeneca è un fiasco sugli anziani? Fonti del governo tedesco parlano di un’efficacia dell’8%
- Vaccini, von der Leyen chiama AstraZeneca: «Rispettare i tempi». Per l’Europa gli obiettivi non cambiano, ma la strada è tutta in salita
- Rinvio per gli over 80 e niente priorità per i prof: l’effetto dei tagli ai vaccini di Pfizer e AstraZeneca, che allontanano l’immunità
- Vaccini, la Commissione europea convoca una riunione d’urgenza sul caso AstraZeneca. Conte: «All’Italia 3,4 milioni di dosi anziché 8»
- Il punto dell’Iss, Locatelli: «Vaccini? Secondi in Ue nonostante i tagli. Con le riduzioni AstraZeneca rimodulare la campagna»
